來源:米內網
精彩內容
1月20日,恆瑞醫藥公告稱,公司的鹽酸右美託咪定注射液通過一致性評價,為國內第3家。米內網數據顯示,該產品在2019年中國公立醫療機構終端銷售額超過35億元。此外,公司3類仿製藥鹽酸右美託咪定氯化鈉注射液進入行政審批階段,有望拿下首仿。
鹽酸右美託咪定是一種相對選擇性α2-腎上腺素受體激動劑,適用於行全身麻醉的手術患者氣管插管和機械通氣時的鎮靜、用於重症監護治療期間開始插管和使用呼吸機患者的鎮靜。鹽酸右美託咪定注射液由Oricon Pharma與雅培聯合研發,最早於1999年12月獲得FDA批準上市。
目前國內已有11家仿製藥企業擁有鹽酸右美託咪定注射液生產批文,米內網數據顯示,該產品在2019年中國城市公立醫院、縣級公立醫院、城市社區中心以及鄉鎮衛生院(簡稱中國公立醫療機構)終端銷售額超過35億元,2020年上半年受疫情影響增速有所下滑。
鹽酸右美託咪定注射液一致性評價申報情況(含新分類報產)
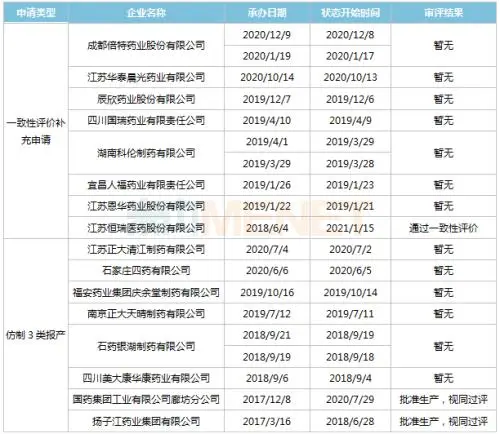
來源:MED中國藥品審評數據庫2.0
米內網數據顯示,目前有8家企業提交鹽酸右美託咪定注射液一致性評價補充申請,恆瑞醫藥的產品已經順利過評;8家企業以仿製3類提交鹽酸右美託咪定注射液上市申請,揚子江、國藥的產品已獲批生產並視同過評。
鹽酸右美託咪定注射液為4+7集採及聯盟集採品種,揚子江藥業的產品因獨家過評“躺贏”市場,在中國公立醫療機構終端的市場份額由2018年的0.22%上升至2020年上半年的84.28%,而原本佔主導地位的恆瑞醫藥,因為產品未過評而不能參與競標,如今公司的產品順利過評,獲得了該品種下一輪的競標機會。
此外,恆瑞醫藥按仿製3類報產的鹽酸右美託咪定氯化鈉注射液已於1月11日進入行政審批階段,該產品由Hospira開發,最早於2013年在美國獲批,目前國內還未有仿製藥獲批上市。在右美託咪定市場競爭上,恆瑞醫藥能否實現“翻盤”?我們拭目以待!
來源:米內網數據庫、上市公司公告等
注:數據統計截至1月20日,如有疏漏,歡迎指正!
轉載請超鏈接註明:頭條資訊 » 35億注射劑揚子江危險!恆瑞過評了 首仿將獲批
免責聲明
:非本網註明原創的信息,皆為程序自動獲取互聯網,目的在於傳遞更多信息,並不代表本網贊同其觀點和對其真實性負責;如此頁面有侵犯到您的權益,請給站長發送郵件,並提供相關證明(版權證明、身份證正反面、侵權鏈接),站長將在收到郵件24小時內刪除。